Autor : Magdalena Kopystyńska
2021-11-25 13:09
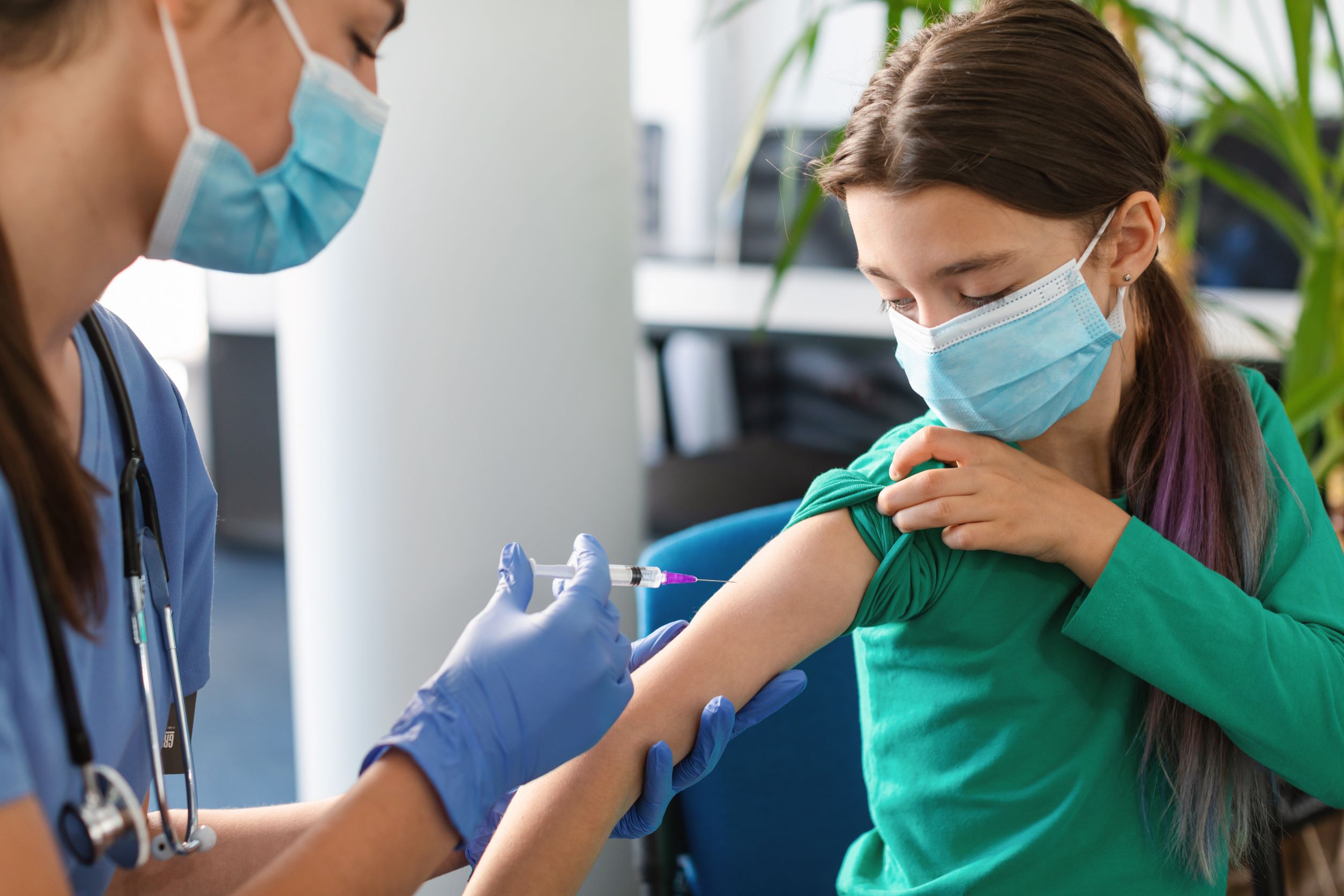
Europejska Agencja Leków wydała pozytywną rekomendację dla szczepionki firmy Pfizer dla dzieci powyżej 5 roku życia. Oznacza to, że dopuściła ten preparat do szczepień dzieci, które do tej pory nie mogły być szczepione.
U dzieci w wieku od 5 do 11 lat dawka preparatu Comirnaty będzie niższa niż stosowana u osób w wieku 12 lat i starszych (10 µg w porównaniu z 30 µg). Podobnie jak w starszej grupie wiekowej, lek podaje się w dwóch wstrzyknięciach w mięsień górnej części ramienia, w odstępie trzech tygodni.
W badaniu dzieci w wieku od 5 do 11 lat wykazano, że odpowiedź immunologiczna na lek Comirnaty podawany w mniejszej dawce w tej grupie wiekowej była porównywalna z odpowiedzią obserwowaną w przypadku większej dawki u osób w wieku od 16 do 25 lat (mierzoną poziomem przeciwciał przeciwko SARS-CoV-2). Skuteczność Comirnaty badano u prawie 2 tys. dzieci w wieku od 5 do 11 lat, u których nie stwierdzono oznak wcześniejszego zakażenia. Dzieci te otrzymały albo szczepionkę albo placebo. Spośród 1 305 dzieci otrzymujących szczepionkę u trzech rozwinęła się choroba COVID-19, w porównaniu z 16 z 663 dzieci, które otrzymały placebo. Oznacza to, że w tym badaniu szczepionka była skuteczna w 90,7% w zapobieganiu COVID-19 (chociaż rzeczywisty wskaźnik mógł wynosić od 67,7% do 98,3%).
Najczęstsze działania niepożądane u dzieci w wieku od 5 do 11 lat są podobne do tych występujących u osób w wieku 12 lat i starszych. Obejmują one ból w miejscu wstrzyknięcia, zmęczenie, ból głowy, zaczerwienienie i obrzęk w miejscu wstrzyknięcia, ból mięśni i dreszcze. Działania te są zwykle łagodne lub umiarkowane i ustępują w ciągu kilku dni po szczepieniu.
W komunikacie agencji czytamy, że w opinii Komitetu ds. Leków dla Ludzi korzyści ze stosowania szczepionki Comirnaty u dzieci w wieku od 5 do 11 lat przewyższają ryzyko, zwłaszcza u tych dotkniętych schorzeniami zagrożonymi ciężkim przebiegiem COVID-19. Bezpieczeństwo i skuteczność szczepionki zarówno u dzieci, jak i u dorosłych będą nadal ściśle monitorowane w miarę jej stosowania w kampaniach szczepień w państwach członkowskich UE za pośrednictwem unijnego systemu nadzoru nad bezpieczeństwem farmakoterapii oraz trwających i dodatkowych badań prowadzonych przez firmę i władze europejskie.
EMA przekaże teraz rekomendację do Komisji Europejskiej, która wyda ostateczną decyzję.
Czytaj także:
 EMA bada kolejną szczepionkę przeciw COVID-19 dla dzieci
EMA bada kolejną szczepionkę przeciw COVID-19 dla dzieci
 Na gwiazdkę dzieci dostaną szczepionkę? Tak chciałby MZ
Na gwiazdkę dzieci dostaną szczepionkę? Tak chciałby MZ
 Koronawirus - co ze szczepieniem dzieci 5+ w Europie?
Koronawirus - co ze szczepieniem dzieci 5+ w Europie?
 Pfizer i BioNTech o szczepionce dla dzieci: bezpieczna i skuteczna
Pfizer i BioNTech o szczepionce dla dzieci: bezpieczna i skuteczna
magdalena.kopystynska@cowzdrowiu.pl