Autor : Aleksandra Kurowska
2023-06-16 17:36
Jest już projekt lipcowej listy leków refundowanych dotyczący m.in. szpiczaka i amyloidozy. Zmiany dotyczą też wyrobów medycznych stosowanych w leczeniu ran. Wśród zmian w lekach aptecznych warto wymienić m.in. dodanie wskazania pozarejestracyjnego (off-label) dla aż 238 leków stosowanych w nadciśnieniu tętniczym. Z kolei w przypadku raka piersi trwają jeszcze ostatnie rozmowy dotyczące dopisania nowych terapii.
PROJEKT OBWIESZCZENIA REFUNDACYJNEGO NR 70 (1 LIPCA 2023 r.)
O tym, że projekt ukaże się dziś i będzie zawierać zmiany dotyczące opatrunków pisaliśmy dziś w tekście, w którym wypowiada się wiceminister Maciej Miłkowski oraz eksperci:
 Projekt listy refundacyjnej: ważne zmiany w finansowaniu opatrunków
Projekt listy refundacyjnej: ważne zmiany w finansowaniu opatrunków
Kilka godzin później ukazała się nowa lista - ale to dopiero projekt, co zaznacza MZ. Więc możliwe, że trafią na nią jeszcze kolejne terapie, jeśli firmy ustąpią więcej w negocjacjach. Nadal trwają prace administracyjne nad finalnym wykazem refundowanych leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych obowiązującym od 1 lipca 2023 r. Wśród nich, prowadzone są intensywne działania w kierunku udostępnienia nowych terapii w leczeniu raka piersi. Niemniej, ich implementacja uzależniona jest od poziomu zaangażowania wszystkich podmiotów odpowiedzialnych partycypujących w obecnym programie lekowym B.9. FM - Leczenie chorych na raka piersi (ICD-10: C50).
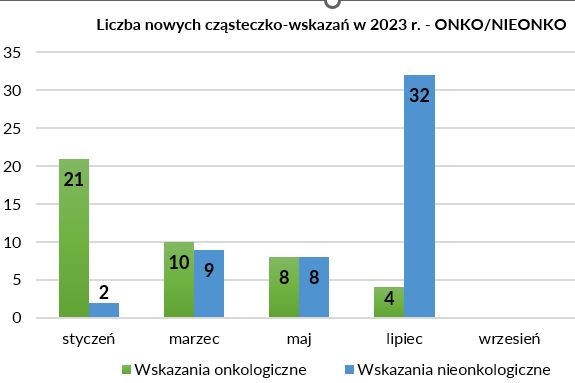
Uwzględniając niniejszy projekt, od początku roku 2023, finansowaniem ze środków publicznych zostanie objętych 94 nowych cząsteczko – wskazań, w tym:
· 43 cząsteczko – wskazania onkologiczne,
· 51 cząsteczko - wskazań nieonkologicznych,
· 31 cząsteczko - wskazania dedykowane chorobom rzadkim.
Najwięcej nowych cząsteczko - wskazań onkologicznych w 2023 r. obserwujemy w hematoonkologii (24), w nowotworach układu oddechowego (8) i urologicznego (5). Najwięcej nowych cząsteczko - wskazań nieonkologicznych w 2023 r. obserwujemy w kardiologii (19), reumatologii (6), hematologii (4), gastroenterologii (4) i dermatologii (4).
Planowany termin publikacji obwieszczenia Ministra Zdrowia w sprawie wykazu refundowanych leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych to 20 czerwca 2023 r.
NOWE WSKAZANIA ORAZ ZMIANY W PROGRAMACH LEKOWYCH i CHEMIOTERAPII
Programy lekowe i chemioterapia | |||||
Nowe wskazania onkologiczne | |||||
Lp. | Nazwa leku | Substancja czynna | Numer programu lekowego/załącznika chemioterapii | Nazwa programu lekowego/ Załącznika chemioterapii | Doprecyzowanie wskazania |
1. | Sarclisa | izatuksymab | B.54 | LECZENIE CHORYCH NA SZPICZAKA PLAZMOCYTOWEGO (ICD-10: C90.0) | Leczenie izatuksymabem w skojarzeniu z pomalidomidem i deksametazonem (schemat IsaPd) od III linii leczenia dorosłych chorych na opornego lub nawrotowego szpiczaka plazmocytowego z niewydolnością nerek (RI), i u których w którymkolwiek z poprzedzających protokołów leczenia zastosowano lenalidomid i inhibitor proteasomu. (Choroba rzadka) |
2. | Kyprolis | karfilzomib | B.54 | LECZENIE CHORYCH NA SZPICZAKA PLAZMOCYTOWEGO (ICD-10: C90.0) | Leczenie karfilzomibem w skojarzeniu z lenalidomidem i deksametazonem (schemat KRd) dorosłych chorych na opornego lub nawrotowego szpiczaka plazmocytowego w II-IV linii leczenia (tj. rozszerzenie dotychczas refundowanego wskazania w schemacie KRd). (Choroba rzadka) |
3. | Darzalex | daratumumab | B.145 | LECZENIE CHORYCH NA UKŁADOWĄ AMYLOIDOZĘ ŁAŃCUCHÓW LEKKICH (AL) (ICD-10: E85.8) | Leczenie daratumumabem w skojarzeniu z bortezomibem, cyklofosfamidem i deksametazonem (schemat D-VCd) w I linii leczenia dorosłych chorych na układową amyloidozę łańcuchów lekkich (AL). (Choroba rzadka) |
4. | Brukinsa | zanubrutynib | B.146 | LECZENIE CHORYCH NA MAKROGLOBULINEMIĘ WALDENSTRÖMA (ICD-10: C88.0) | Leczenie zanubrutynibem w monoterapii dorosłych chorych na makroglobulinemię Waldenströma, wcześniej nieleczonych i niekwalifikujących się do immunochemioterapii albo po wcześniejszej co najmniej 1 linii leczenia. (Choroba rzadka) |
Nowe wskazania nieonkologiczne | |||||
Lp. | Nazwa leku | Substancja czynna | Numer programu lekowego/załącznika chemioterapii | Nazwa programu lekowego/ Załącznika chemioterapii | Doprecyzowanie wskazania |
1. | Mavenclad | kladrybina | B.29 | LECZENIE CHORYCH NA STWARDNIENIE ROZSIANE (ICD-10: G35) | Leczenie kladrybiną w I linii pacjentów z rzutowo-remisyjną postacią stwardnienia rozsianego (RRMS). I linia leczenia zdefiniowana jako wystąpienie minimum 2 rzutów klinicznych niezależnie od zmian MRI w okresie 12 miesięcy przed kwalifikacją. |
2. | Ocrevus | okrelizumab | B.29 | LECZENIE CHORYCH NA STWARDNIENIE ROZSIANE (ICD-10: G35) | Leczenie okrelizumabem w I linii pacjentów z rzutowo-remisyjną postacią stwardnienia rozsianego (RRMS). I linia leczenia zdefiniowana jako wystąpienie minimum 1 rzutu klinicznego albo co najmniej 1 nowe ognisko GD+ w okresie 12 miesięcy przed kwalifikacją. |
3. | Jyseleca | filgotynib | B.33 | LECZENIE CHORYCH Z AKTYWNĄ POSTACIĄ REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW (ICD-10: M05, M06, M08) | Leczenie chorych z RZS kolejnym lekiem z grupy inhibitorów kinaz janusowych (JAK). |
4. | Cosentyx | sekukinumab | B.33 | LECZENIE CHORYCH Z AKTYWNĄ POSTACIĄ REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW (ICD-10: M05, M06, M08) | Leczenie chorych z MIZS: w zapaleniu stawów z zapaleniem przyczepów ścięgien (ERA) i młodzieńczym łuszczycowym zapaleniem stawów (MŁZS)-kolejnym inhibitorem interleukin (IL-17A). |
5. | Xeljanz | tofacytynib | B.36 | LECZENIE CHORYCH Z AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10: M45) | Leczenie chorych z ZZSK-kolejnym lekiemz grupy inhibitorów kinaz janusowych (JAK). |
6. | Ofev | nintedanib | B.135 | LECZENIE PACJENTÓW Z CHOROBĄ ŚRÓDMIĄŻSZOWĄ PŁUC (ICD-10: D86, J67.0-J67.9, J84.1, J84.8, J84.9, J99.0, J99.1, M34) | Leczenie pacjentów z chorobą śródmiąższową płuc przebiegającą z włóknieniem o fenotypie postępującym (PF-ILD). |
7. | Spravato | esketamina | B.147 | LECZENIE CHORYCH NA DEPRESJĘ LEKOOPORNĄ (ICD-10: F33.1, F33.2) | Leczenie esketaminą depresji lekoopornej zdefiniowanej jako zaburzenia depresyjne u osób dorosłych, u których nie wystąpiła odpowiedź na co najmniej dwa różne leki przeciwdepresyjne w obecnym epizodzie depresji o stopniu nasilenia od umiarkowanego do ciężkiego. |
Zmiany w programach lekowych i chemioterapii | |||
Lp. | Numer programu lekowego lub numeru załącznika | Nazwa programu lekowego lub załącznika chemioterapii | Krótki opis zmian dokonanych w obrębie programu lekowego / załącznika chemioterapii |
1. | B.85 | LECZENIE PACJENTÓW Z GRUCZOLAKORAKIEM TRZUSTKI (ICD-10: C25.0, C25.1, C25.2, C25.3, C25.5, C25.6, C25.7, C25.8, C25.9) | Zmiana sposobu potwierdzania mutacji germinalnej BRCA1/BRCA2. |
2. | B.135 | LECZENIE PACJENTÓW Z CHOROBĄ ŚRÓDMIĄŻSZOWĄ PŁUC (ICD-10: D86, J67.0-J67.9, J84.1, J84.8, J84.9, J99.0, J99.1, M34) | Zmiany w programie lekowym o charakterze porządkującym. Rozszerzenie populacji o pacjentów z chorobą śródmiąższową płuc przebiegającą z włóknieniem o fenotypie postępującym (PF-ILD). |
NOWE WSKAZANIA ORAZ ZMIANY W REFUNDACJI APTECZNEJ
Apteka | ||||
Nowe wskazania refundacyjne | ||||
Lp. | Nazwa leku, środka spożywczego specjalnego przeznaczenia lub wyrobu medycznego | Substancja czynna | Wskazanie refundacyjne | Doprecyzowanie wskazania |
1. | Acarizax | standaryzowany wyciąg alergenowy roztoczy kurzu domowego (Dermatophagoides pteronyssinus, Dermatophagoides farina) | Leczenie młodzieży w wieku od ukończonego 12. roku życia do ukończonego 17. roku życia z umiarkowanym lub ciężkim alergicznym nieżytem nosa spowodowanym kurzem domowym, utrzymującym się pomimo stosowania leków łagodzących objawy, u których rozpoznanie zostało postawione na podstawie wywiadu klinicznego oraz dodatniego testu alergicznego na roztocza kurzu domowego (punktowe testy skórne i /lub swoiste immunoglobuliny E) | Pierwszy refundowany produkt w postaci liofilizatu doustnego stanowiący wyciąg alergenowy roztoczy kurzu domowego |
2. | Detriol | kalcytriol | We wszystkich zarejestrowanych wskazaniach na dzień wydania decyzji | Wskazanie do stosowania u osób dorosłych w: · ciężkiej lub postępującej wtórnej nadczynności przytarczyc prowadzącej do osteodystrofii nerkowej z umiarkowaną lub ciężką przewlekłą niewydolnością nerek, · hipokalcemii spowodowanej niedoczynnością przytarczyc (pooperacyjna, idiopatyczna i rzekoma niedoczynność przytarczyc), · dziedzicznej krzywicy hipofosfatemicznej. |
3. | Findarts Duo | dutasteryd+ tamsulozyna | Leczenie umiarkowanych do ciężkich objawów łagodnego rozrostu gruczołu krokowego | Pierwszy lek refundowany stanowiący połączenie - blokera receptora alfa-adrenergicznego z inhibitorami 5-alfa reduktazy. |
4. | Influvac Tetra | vaccinum influenzae inactivatum ex corticis antigeniis praeparatum Szczepionka przeciw grypie (antygen powierzchniowy), inaktywowana | We wszystkich zarejestrowanych wskazaniach na dzień wydania decyzji | Profilaktyka grypy, zwłaszcza u osób o zwiększonym ryzyku wystąpienia powikłań pogrypowych. Influvac Tetra jest wskazany dla osób dorosłych i dzieci w wieku od 6 miesięcy. Influvac Tetra powinien być stosowany zgodnie z oficjalnymi zaleceniami. |
5. | Tresiba | insulina degludec | Cukrzyca typu I u dorosłych; cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥7,5% oraz cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca o znanej przyczynie (zgodnie z definicją wg WHO); cukrzyca typu I u dzieci powyżej 1. roku życia i młodzieży; cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥7,5% oraz cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca u dzieci powyżej 1. roku życia i młodzieży o znanej przyczynie (zgodnie z definicją wg WHO) | Podskórna, długodziałająca insulina bazowa degludec bez skojarzenia z dodatkową substancją czynną o działaniu hipoglikemizującym. W przeszłości produkt refundowany w dwóch innych prezentacjach, których refundacja została zaprzestana na skutek decyzji podmiotu odpowiedzialnego. Redukcja kryterium kwalifikującego do leczenia - poziomu hemoglobiny glikowanej, o 0,5 punktu procentowego (z ≥8% na ≥7,5%). |
6. | Trixeo Aerosphere | formoterol fumaranu dwuwodnego + bromek glikopironiowy + budezonid | Leczenie podtrzymujące u pacjentów dorosłych z umiarkowaną lub ciężką przewlekłą obturacyjną chorobą płuc (POChP) | Leczenie podtrzymujące u pacjentów dorosłych z umiarkowaną lub ciężką przewlekłą obturacyjną chorobą płuc (POChP), u których nie uzyskuje się odpowiedniego efektu leczenia podczas jednoczesnego stosowania kortykosteroidu wziewnego i długo działającego agonisty receptorów beta 2 lub jednoczesnego stosowania długo działającego agonisty receptorów beta 2 i długo działającego antagonisty receptorów muskarynowych. |
7. | Vimetso | wildagliptyna + chlorowodorek metforminy | We wszystkich zarejestrowanych wskazaniach na dzień wydania decyzji | Stosowanie jako uzupełnienie diety i ćwiczeń fizycznych w celu poprawy kontroli glikemii u osób dorosłych z cukrzycą typu 2: · u pacjentów, u których nie uzyskano wystarczającej kontroli glikemii po zastosowaniu chlorowodorku metforminy w monoterapii, · u pacjentów już leczonych wildagliptyną w skojarzeniu z chlorowodorkiem metforminy, w postaci oddzielnych tabletek, · w skojarzeniu z innymi produktami leczniczymi stosowanymi w leczeniu cukrzycy, w tym z insuliną, gdy produkty te nie zapewniają wystarczającej kontroli glikemii. |
8. | Różne produkty handlowe | amlodypina + walsartan | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | Dodanie wskazania pozarejestracyjnego (off-label) dla preparatów złożonych, których zastosowanie wg zarejestrowanych wskazań jest ograniczone do wskazań substytucyjnych lub addycyjnych. Rozszerzenie zakresu wskazań refundacyjnych umożliwi rozpoczęcie leczenia nadciśnienia tętniczego od terapii skojarzonej. |
9. | Różne produkty handlowe | amlodypina + walsartan + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
10. | Różne produkty handlowe | kandesartan + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
11. | Różne produkty handlowe | kandesartan + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
12. | Różne produkty handlowe | indapamid + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
13. | Różne produkty handlowe | lizynopryl + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
14. | Różne produkty handlowe | lizynopryl + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
15. | Różne produkty handlowe | losartan + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
16. | Różne produkty handlowe | losartan + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
17. | Różne produkty handlowe | peryndopryl + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
18. | Różne produkty handlowe | peryndopryl + indapamid (bez dawki 2,5+0,625 mg) | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
19. | Różne produkty handlowe | ramipryl + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
20. | Różne produkty handlowe | ramipryl + felodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
21. | Różne produkty handlowe | ramipryl + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
22. | Różne produkty handlowe | telmisartan + amlodypina | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
23. | Różne produkty handlowe | telmisartan + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
24. | Różne produkty handlowe | walsartan + hydrochlorotiazyd | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
25. | Różne produkty handlowe | telmisartan + indapamid | Nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL. | |
Zmiany na liście 75+ | |||
Lp. | Substancja czynna | Wskazanie refundacyjne | Dodatkowe informacje |
1. | insulina degludec | Cukrzyca typu I u dorosłych; cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥7,5% oraz cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca o znanej przyczynie (zgodnie z definicją wg WHO); cukrzyca typu I u dzieci powyżej 1. roku życia i młodzieży; cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥7,5% oraz cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca u dzieci powyżej 1. roku życia i młodzieży o znanej przyczynie (zgodnie z definicją wg WHO) | Zwiększenie dostępności refundacyjnej do leczenia długodziałającą insuliną degludec w terapii cukrzycy, u pacjentów po ukończeniu 75. roku życia. |
2. | formoterol fumaranu dwuwodnego + bromek glikopironiowy + budezonid | Leczenie podtrzymujące u pacjentów dorosłych z umiarkowaną lub ciężką przewlekłą obturacyjną chorobą płuc (POChP) | Zwiększenie dostępności refundacyjnej do nowej technologii medycznej w leczeniu umiarkowanej lub ciężkiej przewlekłej obturacyjnej choroby płuc (POChP), u pacjentów po ukończeniu 75. roku życia. |
3. | vaccinum influenzae inactivatum ex corticis antigeniis praeparatum Szczepionka przeciw grypie (antygen powierzchniowy), inaktywowana | We wszystkich zarejestrowanych wskazaniach na dzień wydania decyzji | Rozszerzenie wskazania refundacyjnego do pełnego zakresu wskazań zgodnie z rejestracją szczepionki. |
Zmiany na liście Ciąża+ | |||
Lp. | Substancja czynna | Wskazanie refundacyjne | Dodatkowe informacje |
1. | insulina degludec | Cukrzyca typu I u dorosłych; cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥7,5% oraz cukrzyca typu 2 u dorosłych pacjentów leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca o znanej przyczynie (zgodnie z definicją wg WHO); cukrzyca typu I u dzieci powyżej 1. roku życia i młodzieży; cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z HbA1c ≥7,5% oraz cukrzyca typu 2 u dzieci powyżej 1. roku życia i młodzieży leczonych insuliną NPH od co najmniej 6 miesięcy i z udokumentowanymi nawracającymi epizodami ciężkiej lub nocnej hipoglikemii oraz cukrzyca u dzieci powyżej 1. roku życia i młodzieży o znanej przyczynie (zgodnie z definicją wg WHO) | Zwiększenie dostępności refundacyjnej do leczenia długodziałającą insuliną degludec w terapii cukrzycy, u pacjentek w okresie ciąży. |
2. | vaccinum influenzae inactivatum ex corticis antigeniis praeparatum Szczepionka przeciw grypie (antygen powierzchniowy), inaktywowana | We wszystkich zarejestrowanych wskazaniach na dzień wydania decyzji | Rozszerzenie wskazania refundacyjnego do pełnego zakresu wskazań zgodnie z rejestracją szczepionki. |
INFORMACJA DOTYCZĄCA ZMIAN W KATEGORYZACJI OPATRUNKÓW SPECJALISTYCZNYCH
Od 1 lipca 2023 r. planowane jest przyjęcie nowej kategoryzacji opatrunków specjalistycznych dostępnych w aptece na receptę, co doprowadzi do wyróżnienia 30 grup limitowych. Obecnie opatrunki specjalistyczne skategoryzowane są w 14 grupach limitowych. Konsekwencją rozszerzenia grup limitowych będzie precyzyjne klasyfikowanie poszczególnych produktów pod względem technologicznym.
69W (obecnie) |
| 70W (projekt obwieszczenia) | ||
Identyfikator grupy limitowej | Nazwa grupy limitowej | Identyfikator grupy limitowej | Nazwa grupy limitowej | |
220.1 | Opatrunki alginianowe i hydrowłókienne | 261.1 | Opatrunki do ran z wysiękiem - opatrunki alginianowe | |
220.2 | Opatrunki hydrokoloidowe | 261.2 | Opatrunki do ran z dużym wysiękiem - o właściwościach absorpcji płynu wysiękowego bezpośrednio do wnętrza struktury włókna | |
220.3 | Opatrunki regulujące poziom wilgotności rany z dodatkami | 261.3 | Opatrunki do ran z wysiękiem - o właściwościach umożliwiających zachowanie stałego, wilgotnego środowiska wewnątrz rany dzięki wykorzystaniu budowy lipidowej | |
220.4 | Opatrunki poliuretanowe | 261.4 | Opatrunki do ran z wysiękiem - o właściwościach umożliwiających zachowanie stałego, wilgotnego środowiska wewnątrz rany dzięki wykorzystaniu budowy lipidowej z dodatkiem nanooligosacharydów | |
220.5 | Opatrunki hydrożelowe | 261.5 | Opatrunki do ran z wysiękiem - piankowe z warstwami funkcjonalnymi | |
220.6 | Opatrunki regulujące poziom wilgotności rany | 261.6 | Opatrunki do ran z wysiękiem i podatnych na uszkodzenie – piankowe posiadające silikonową warstwę kontaktową | |
220.7 | Opatrunki przeciwbakteryjne zawierające jony srebra | 261.7 | Opatrunki niechłonne do ran podatnych na uszkodzenie – piankowe przekazujące wysięk do opatrunku wtórnego, posiadające warstwy funkcjonalne | |
220.8 | Opatrunki z węglem aktywowanym | 261.8 | Opatrunki niechłonne do ran podatnych na uszkodzenie – siatkowe przekazujące wysięk do opatrunku wtórnego, posiadające dodatkowe właściwości funkcjonalne | |
220.9 | Opatrunki kolagenowe | 261.9 | Opatrunki do ran z wysiękiem - z pianki poliuretanowej z kalaminą lub cynkiem oraz kohezyjną opaską kompresyjną | |
220.10 |
| 261.10 | Opatrunki do mechanicznego oczyszczania rany - z mikrowłókniny z kwasem hialuronowym i fosfolipidami | |
220.12 | Opatrunki w postaci żelu | 261.11 | Opatrunki do ran z wysiękiem i podatnych na uszkodzenie – piankowe posiadające hydrożelową warstwę kontaktową | |
220.13 | Opatrunki przeciwbakteryjne zawierające nanokrystaliczne srebro | 262.1 | Opatrunki wysokochłonne do ran z wysiękiem – o właściwościach wysokiej absorbcji i retencji wysięku dzięki wykorzystaniu superabsorbentu | |
220.14 | Opatrunki przeciwbakteryjne zawierające jony srebra regulujące poziom wilgotności rany | 262.2 | Opatrunki wysokochłonne do ran z wysiękiem – o właściwościach wysokiej absorbcji i retencji wysięku dzięki wykorzystaniu superabsorbentu, posiadające silikonową warstwę kontaktową | |
220.15 | Opatrunki biopolimerowe | 263.1 | Opatrunki do ran wymagających aktywnego oczyszczania – o działaniu płuczącym i absorpcyjnym | |
|
| 263.2 | Opatrunki w postaci pasty lub żelu bez substancji przeciwdrobnoustrojowych | |
264.1 | Opatrunki chłonne do ran zakażonych z wysiękiem - piankowe z zawartością PHMB | |||
264.2 | Opatrunki niechłonne do ran zakażonych – z substancją przeciwdrobnoustrojową w postaci srebra nanokrystalicznego | |||
264.3 | Opatrunki niechłonne do ran zakażonych - siatkowe zawierające PVP-jod i glikol polietylenowy | |||
264.4 | Opatrunki chłonne z węglem aktywowanym | |||
264.5 | Opatrunki do ran zakażonych ze srebrem metalicznym | |||
264.6 | Opatrunki do ran zakażonych z kwasem hialuronowym i dichlorowodorkiem oktenidyny | |||
265.1 | Opatrunki wysokochłonne do ran zakażonych z wysiękiem o właściwościach żelujących, absorbujących lub zatrzymujących wysięk w strukturze włókna - ze srebrem | |||
265.2 | Opatrunki wysokochłonne do ran zakażonych z wysiękiem - piankowe z warstwami funkcjonalnymi i srebrem | |||
265.3 | Opatrunki do ran zakażonych z wysiękiem - z aktywnym węglem i srebrem | |||
265.4 | Opatrunki do ran zakażonych z wysiękiem- alginianowe ze srebrem | |||
266.1 | Opatrunki w postaci pasty, maści lub żelu - zawierające substancje przeciwdrobnoustrojowe | |||
267.1 | Opatrunki do ran z wysiękiem bez cech infekcji - zawierające kolagen | |||
267.2 | Opatrunki hydrokoloidowe do ran bez cech infekcji, z wysiękiem – o właściwościach żelujących w kontakcie z wysiękiem | |||
267.3 | Opatrunki biowchłanialne do ran bez cech infekcji | |||
268.1 | Opatrunki do ran wymagających odpowiedniego poziomu uwodnienia – o właściwościach nawilżających i absorpcyjnych | |||
Powyższa klasyfikacja opiera się na określeniu stanu mikrobiologicznego rany, stopnia wysięku oraz zróżnicowania opatrunków pod względem technologicznym. Zaimplementowanie przedmiotowej zmiany spowoduje znaczny spadek dopłat pacjentów do refundowanych opatrunków specjalistycznych w porównaniu z dotychczas obowiązującym podziałem. Szacowane oszczędności dla polskich pacjentów wzrosną o prawie 20% w porównaniu do aktualnego scenariusza i wyniosą ok. 7,96 mln zł rocznie.
Koordynacja wielopłaszczyznowych działań wprowadzających nową kategoryzację opatrunków specjalistycznych stanowiła ogromne wyzwanie, bowiem wymagała wszczęcia 477 postepowań administracyjnych w zakresie zmian obowiązujących dotychczas decyzji refundacyjnych. Realizacja przedsięwziętych założeń we wspomnianym zakresie jest przykładem wzorowej współpracy Ministerstwa Zdrowia, Agencji Oceny Technologii Medycznych i Taryfikacji oraz podmiotów odpowiedzialnych zaangażowanych w dostarczanie refundowanych opatrunków specjalistycznych.
INFORMACJA DOTYCZĄCA WSKAZANIA OFF-LABEL ZŁOŻONYCH LEKÓW HIPOTENSYJNYCH
We współpracy z Konsultantem Krajowym w dziedzinie hipertensjologii od 1 lipca 2023 r. planowane jest rozszerzenie zakresu wskazań refundacyjnych wobec 238 produktów złożonych o działaniu hipotensyjnym zawierających wymienione powyżej substancje czynne o wskazanie pozarejestracyjne „nadciśnienie tętnicze u osób dorosłych, w przypadkach innych niż określono w ChPL”. Nowe wskazanie umożliwi stosowanie hipotensyjnych leków złożonych zgodnie z najnowszymi wytycznymi klinicznymi, tj. już w momencie rozpoczynania terapii, a także w momencie jej zmiany i intensyfikowania leczenia. Zdaniem ekspertów klinicznych stosowanie produktów dwu- lub trójskładnikowych poprawia szeroko pojętą efektywność terapii nadciśnienia tętniczego. Przedmiotowe rozszerzenie wskazań refundacyjnych wieloskładnikowych leków stosowanych w nadciśnieniu tętniczym, stanowi największą zmianę w dziedzinie hipertensjologii na przełomie ostatnich lat. Nowy paradygmat leczenia nadciśnienia tętniczego zapewni lepszy poziom współpracy pacjenta z lekarzem (compliance) i postępowanie zgodne z nowymi rekomendacjami klinicznymi.
Materiały
70-Podstawy-limitu-apteka
70-Podstawy-limitu-apteka.xlsx 0.06MB
70-Projekt-załącznika-do-obwieszczenia
70-Projekt-załącznika-do-obwieszczenia.pdf 79.43MB
70-Projekt-załącznika-do-obwieszczenia
70-Projekt-załącznika-do-obwieszczenia.xlsx 0.73MB
70-Zmiany-cen-detalicznych-i-dopłat-pacjenta
70-Zmiany-cen-detalicznych-i-dopłat-pacjenta.xlsx 0.11MB
Redaktor naczelna, od ponad 20 lat pracuje w mediach. Była redaktor naczelna Polityki Zdrowotnej, redaktor m.in. w Rzeczpospolitej, Dzienniku Gazecie Prawnej. Laureatka branżowych nagród dla dziennikarzy i mediów medycznych oraz Polskiej Izby Ubezpieczeń. Kontakt: aleksandra.kurowska@cowzdrowiu.pl